PLGA@Rapamycin(聚乳酸-羟基乙酸共聚物包载雷帕霉素)是一种基于生物可降解聚合物的药物递送系统,通过将免疫抑制剂雷帕霉素(Rapamycin)包裹在PLGA纳米粒或微球中,实现药物的缓释、靶向递送及Therapeutic effect 优化。
一、改进制备工艺参数
优化乳化-溶剂挥发法的关键参数
该方法是制备 PLGA@Rapamycin 的常用技术,核心是减少药物在水相中的扩散损失:
提高有机相/水相比例:增加有机相(如二氯甲烷)比例(如从 1:5 提升至 1:2),可减少药物因分配系数差异向水相的迁移,负载量可提高 10%-15%(但需注意乳化稳定性,比例过高可能导致乳液分层)。
选择合适的乳化剂及浓度:
优先使用低浓度(0.5%-1%)的非离子型乳化剂(如 PVA 8000),其对疏水性药物的干扰较小,相比高浓度乳化剂(如 5% PVA)可减少药物与乳化剂的非特异性结合,负载量提升约 10%。
采用复合乳化剂(如 PVA + 吐温 80,比例 3:1),可进一步稳定油滴,减少药物泄露。
调控搅拌速率与乳化时间:
中等搅拌速率(500-1000 rpm)可形成尺寸适中的油滴(1-5 μm),药物包裹更充分;过高速率(>2000 rpm)可能导致油滴破裂,药物泄露增加。
延长乳化时间(如从 5 分钟增至 15-20 分钟),使药物在油相中均匀分散,减少局部富集导致的泄露。
采用复乳液法(W/O/W)时的优化
若需包裹少量水溶性辅料(如助溶剂),可采用复乳液法,但需:
减少内水相体积(如内水相/油相比例从 1:3 降至 1:5),降低药物向外部水相的扩散。
在内水相中加入少量 PLGA(如 0.5%),增强界面吸附,减少药物泄露。
二、引入功能性添加剂
添加疏水型增容剂
在 PLGA 有机相中加入少量与雷帕霉素和 PLGA 均兼容的疏水物质,如:
聚己内酯(PCL):与 PLGA 共混(比例 1:9 至 3:7),可提高载体对疏水性药物的容纳能力,负载量提升 15%-25%,同时不明显影响 PLGA 的降解性能。
甘油三酯或脂肪酸酯(如油酸乙酯):作为药物增溶剂,增加雷帕霉素在有机相中的溶解度(从约 10 mg/mL 提升至 20-30 mg/mL),间接提高负载量。
使用离子对试剂
雷帕霉素结构中含弱碱性基团,可与酸性试剂(如十二烷基硫酸钠 SDS)形成离子对,增强其在有机相中的溶解度,同时减少水相迁移,负载量可提升 20% 左右(需注意 SDS 的细胞Poison 性,浓度控制在 0.1% 以下)。
三、调控载体的微观结构
构建多孔 PLGA 载体
通过在制备过程中引入致孔剂(如碳酸氢铵、氯化钠颗粒),形成多孔结构(孔径 1-10 μm),增加载体的比表面积和内部空间,提高药物负载量(可提升 30%-50%)。例如:
在 PLGA 有机相中加入 5%-10% 的碳酸氢铵(粒径 5 μm),乳化后碳酸氢铵在水相中溶解形成孔隙,雷帕霉素可填充于孔隙中,负载量明显提高。
制备核-壳结构或多层包裹
采用层层包裹技术:先制备雷帕霉素-PLGA 纳米粒,再用 PLGA 二次包裹形成核-壳结构,可避免单次包裹时的药物饱和限制,负载量提升 20%-40%。
控制 PLGA 的固化速率:在溶剂挥发过程中,通过梯度降温(如从 37℃降至 25℃)延缓 PLGA 固化,使药物更充分地进入载体内部,减少表面吸附导致的损失。
名称:PLGA@Rapamycin
产品规格:mg/g
纯度:95%+
保存方式:-20℃以下,避光,防潮
保质期限:12个月
用途:科研
温馨提示:仅用于科研,不能用于人体
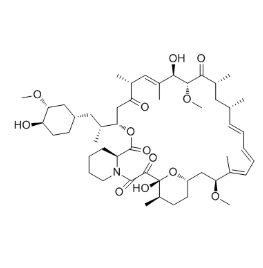
图:Rapamycin

 2025-08-12 作者:ws 来源:
2025-08-12 作者:ws 来源:

