纳米级脂质体:纳米级脂质体主要由磷脂双分子层组成,类似于细胞膜的结构。磷脂分子具有亲水的头部和疏水的尾部,在水中会自发地形成双层结构,将内部的水相空间与外部的水相环境分隔开来。纳米级脂质体的粒径通常在 10 - 1000 纳米之间,这个尺寸范围使得它们具有一些性质,如能够通过增强渗透和保留(EPR)效应在tumor组织中积累、可以被细胞内吞等。根据脂质体的结构和组成,可以分为多层脂质体(MLV)、小单层脂质体(SUV)和大单层脂质体(LUV)等。
微球:微球通常是由高分子材料或无机材料制成的球形颗粒。高分子材料如聚乳酸(PLA)、聚乳酸 - 羟基乙酸共聚物(PLGA)、明胶等,无机材料如二氧化硅、碳酸钙等。微球的粒径一般在 1 - 1000 微米之间,比纳米级脂质体的粒径大得多。微球的结构可以是实心的,也可以是空心的,内部可以包裹药物或其他活性成分。根据微球的制备方法和性质,可以分为聚合物微球、脂质微球、磁性微球等。聚合物微球是由高分子材料制成的,具有良好的生物相容性和可降解性;脂质微球是由脂质材料制成的,类似于脂质体的结构,但粒径较大;磁性微球是含有磁性材料的微球,可以在外加磁场的作用下实现定向递送。

图为:微球
纳米级脂质体与微球制备方法:
纳米级脂质体:
薄膜分散法:将磷脂和胆固醇等脂质溶解在有机溶剂中,然后在旋转蒸发仪上蒸发除去有机溶剂,使脂质在容器壁上形成一层薄膜。接着加入水相溶液,通过搅拌或超声处理等方法使脂质薄膜水化,形成脂质体。
逆相蒸发法:将磷脂等脂质溶解在有机溶剂中,加入含有待包裹物质的水相溶液,然后进行超声处理,形成油包水型乳剂。再蒸发除去有机溶剂,使乳剂中的油滴发生相转变,形成水包油包水型的多层脂质体。最后通过超声处理或挤压等方法得到纳米级脂质体。
乙醇注入法:将磷脂等脂质溶解在乙醇中,然后将乙醇溶液缓慢注入到水相溶液中,通过搅拌或超声处理等方法使乙醇扩散,脂质在水相中自组装形成脂质体。
微球制备方法:
乳化 - 溶剂挥发法:将高分子材料溶解在有机溶剂中,加入含有药物或其他活性成分的水相溶液,通过搅拌或超声处理等方法形成油包水型乳剂。然后将乳剂滴加到含有表面活性剂的水相溶液中,搅拌或超声处理使有机溶剂挥发,高分子材料逐渐固化形成微球。
喷雾干燥法:将含有药物或其他活性成分的高分子材料溶液通过喷雾干燥设备喷成雾状,在热空气的作用下,有机溶剂迅速挥发,高分子材料固化形成微球。
沉淀法:将高分子材料溶解在适当的溶剂中,加入药物或其他活性成分,然后通过改变溶剂的性质或加入沉淀剂等方法,使高分子材料沉淀形成微球。层磷脂双分子层组成,粒径较小且相对均匀。
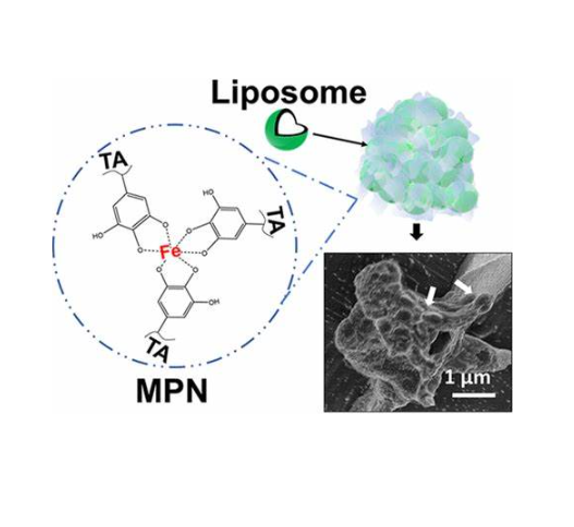
图为:纳米级脂质体
纳米级脂质体与微球的应用:
药物递送:纳米级脂质体和微球都可以作为药物的载体,用于提高药物的稳定性、生物利用度和靶向性。纳米级脂质体主要用于包裹水溶性和脂溶性的药物分子,适用于Treatment tumor、等。微球则适用于包裹大分子药物(如蛋白质、多肽、核酸等)和缓释药物。纳米级脂质体和微球还可以通过联合用药的方式,提高药物的Treatment 效果。例如,将不同作用机制的药物同时包裹在纳米级脂质体或微球中,可以实现协同Treatment 的效果。
成像:纳米级脂质体和微球可以作为成像的造影剂,用于提高成像的对比度和分辨率。纳米级脂质体可以包裹荧光染料、磁共振造影剂等,用于荧光成像、磁共振成像等。微球则可以包裹放射性核素、超声造影剂等,用于核医学成像、超声成像等。纳米级脂质体和微球还可以通过表面修饰连接抗体或配体,实现对特定细胞或组织的靶向成像,提高诊断的准确性和特异性。

 2024-12-18 作者:lkr 来源:
2024-12-18 作者:lkr 来源:

