西安瑞禧生物提供的微米脂质体(巨型单层囊泡),以高分子脂质材料为主要成分,不仅可以用于人造细胞方面的研究,还可以用于药物递送。与传统药物递送系统相比,脂质体这类巨型囊泡具有免疫原性较低/无免疫原性、生物相容性、生物降解性、安全性更好的等优点。微米脂质体(巨型单层囊泡)可用于亲水药物,或蛋白/DNA/RNA等生物活性分子的药物递送,也可负载疏水脂溶性药物分子或荧光染料,为巨型单层囊泡的药物递送应用提供了新的方向。
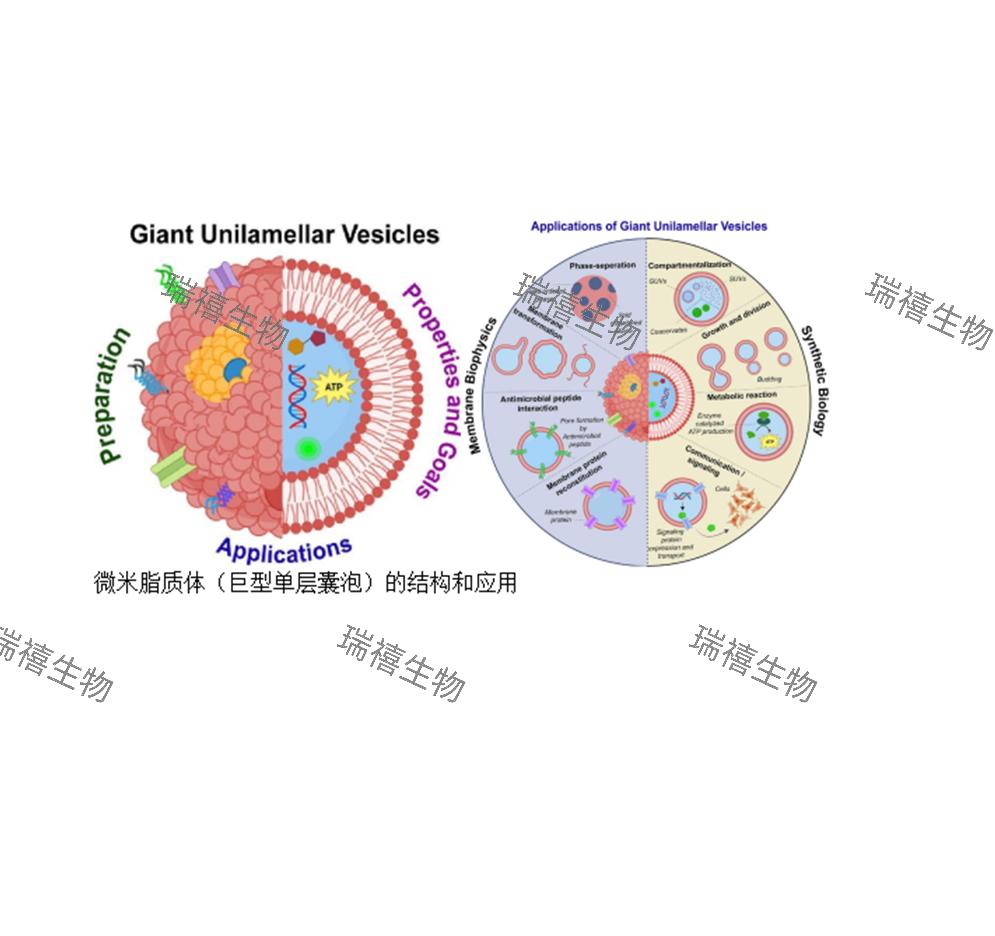
微米脂质体(巨型单层囊泡)的结构和应用
微米脂质体(Giant Unilamellar Vesicles, GUVs)作为直径范围为1-100 μm的巨型单层囊泡,其核心结构由单层磷脂双分子层构成,膜厚度约4-5 nm,与天然细胞膜的脂质组成及拓扑结构高度相似。与纳米脂质体(50-200 nm)相比,GUVs的微米级尺寸赋予其物理化学性质:
1.直接光学可视化:无需荧光标记即可通过相差显微镜、全内反射荧光显微镜(TIRFM)实时观测膜形态(如囊泡融合、出芽、分裂)及膜蛋白动态分布,成为研究膜生物物理学的模型。
2.跨尺度功能集成:单囊泡内可封装体积达皮升级(10⁻¹² L)的生物活性分子(如蛋白质、核酸、酶反应体系),支持多组分共定位与级联反应。
3.半透性膜界面:磷脂双分子层的动态交换特性允许小分子(O₂、CO₂、离子)通过被动扩散自由进出,而大分子(蛋白质、DNA)则被有效滞留,形成"分子筛"效应,为药物递送系统提供时空可控释放的基础。
作为自下而上构建人工细胞的核心元件,GUVs通过模块化设计实现细胞级功能的仿生重构:
1.膜蛋白功能化支架
离子通道整合:将电压门控钾离子通道(KvAP)嵌入GUVs膜,可构建人工电信号传导系统,结合光遗传学工具(如ChR2光敏蛋白)实现光控膜电位调控。
跨膜受体模拟:通过微流控技术将G蛋白偶联受体(GPCR)定向锚定于GUVs表面,结合脂质体-微珠偶联技术,构建可响应肾上腺素等配体的信号转导平台,揭示受体-配体相互作用动力学。
2.细胞器级功能模块化
人工线粒体:在GUVs内封装三羧酸循环关键酶(柠檬酸合酶、异柠檬酸脱氢酶)及NADH荧光探针,通过荧光共振能量转移(FRET)监测代谢流,验证最小代谢单元的可行性。
基因表达系统:将T7 RNA聚合酶、DNA模板及核糖体亚基共封装于GUVs,结合微流控芯片实现mRNA转录-翻译的级联反应,为无细胞蛋白质合成提供封闭反应腔室。
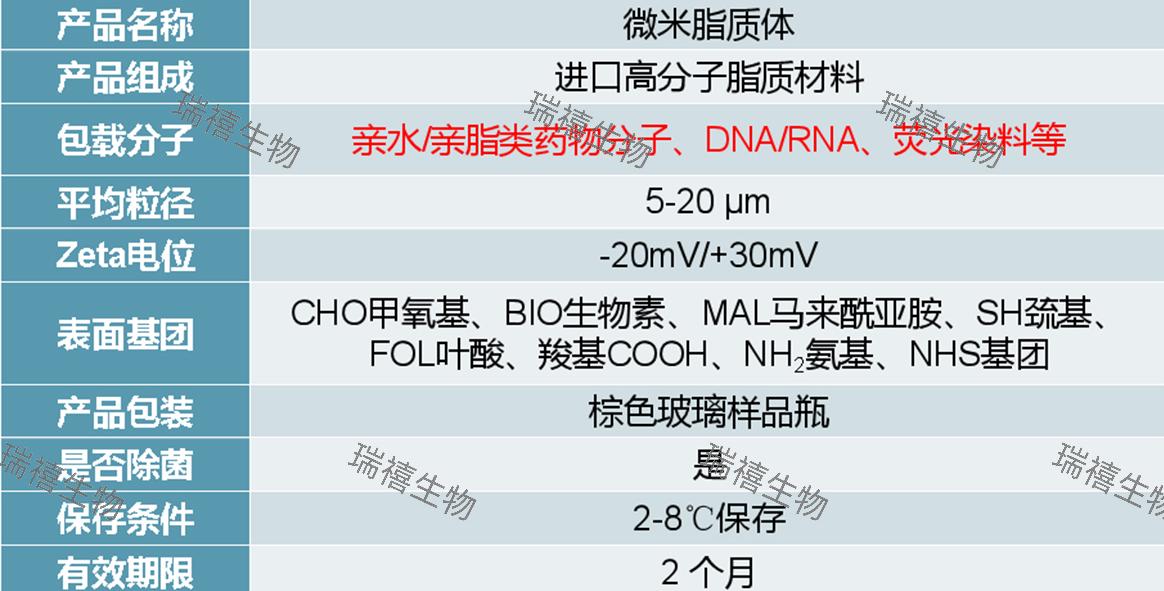

图微米脂质体的激光扫描共聚焦显微镜图像。Cy3标记的水溶性蛋白(黄色),罗丹明B染色的脂质体膜(红色)。共定位显示蛋白被负载至微米脂质体中。

 2025-05-06 作者:wff 来源:
2025-05-06 作者:wff 来源:

