纳米金偶联抗体/蛋白试剂盒通过创新性的化学偶联策略,利用抗体/蛋白分子表面存在的伯胺基团(如赖氨酸侧链的ε-氨基),构建了快速、温和且具有高普适性的共价偶联体系,为生物分子功能化修饰开辟新路径。
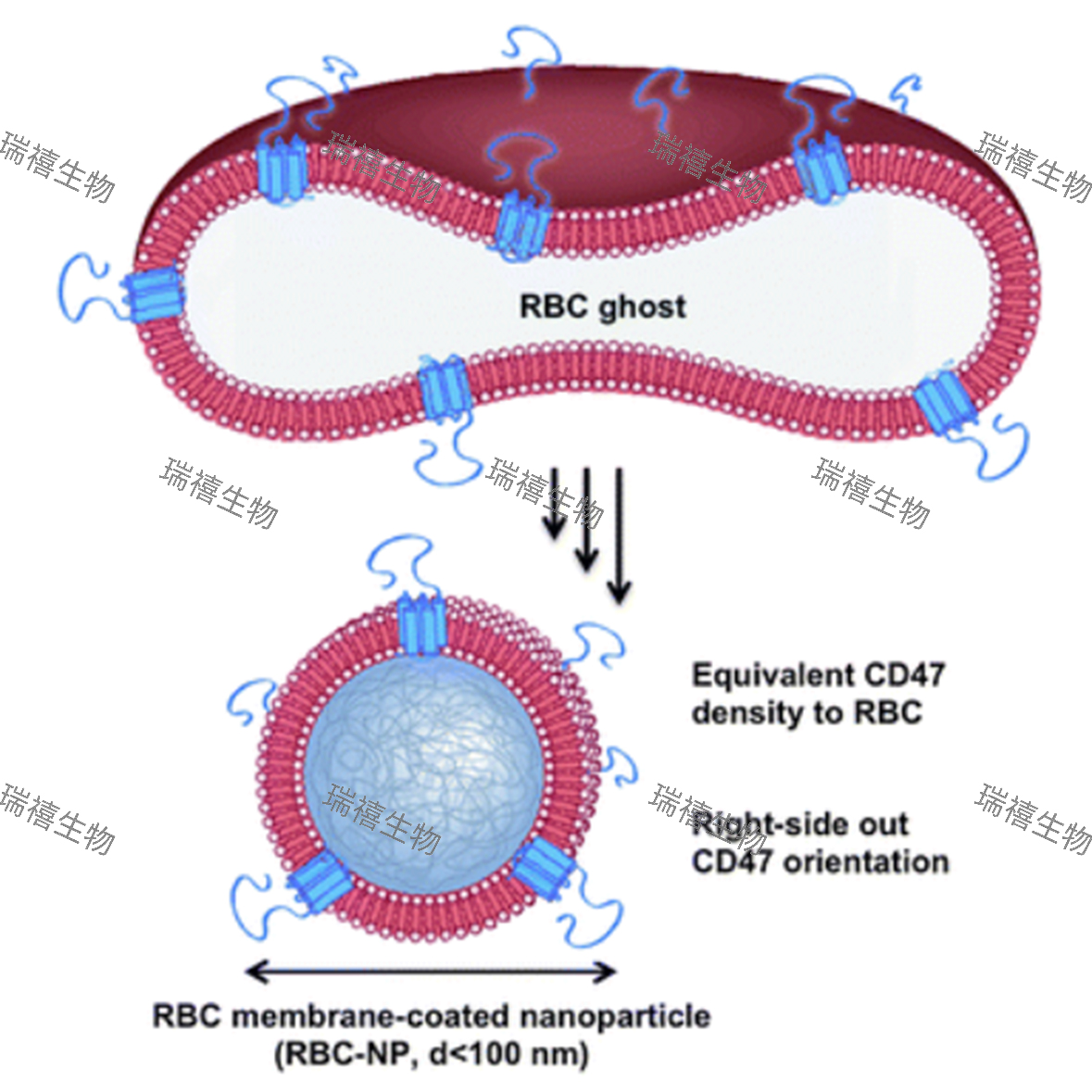
该试剂盒的核心技术依托于纳米金颗粒表面修饰的活性羧基(或磺酸基等)与生物分子伯胺基团之间的特异性共价反应。在温和的缓冲体系(pH 7.0-8.0)中,纳米金表面的羧基经碳二亚胺(EDC)和N-羟基琥珀酰亚胺(NHS)活化后,形成高反应活性的NHS酯中间体,可与抗体/蛋白分子中赖氨酸残基的伯胺基团发生酰胺化反应,形成稳定的共价键。这一过程具有以下优势:
反应条件温和:无需极端pH或有机溶剂,最大程度保留抗体/蛋白的天然构象与生物活性;
反应特异性高:伯胺基团存在于抗体/蛋白表面,但试剂盒通过优化反应动力学,可避免对活性位点的非特异性修饰;
偶联位点可控:通过调节纳米金表面功能基团密度,可实现对偶联位点数量与分布的调控。
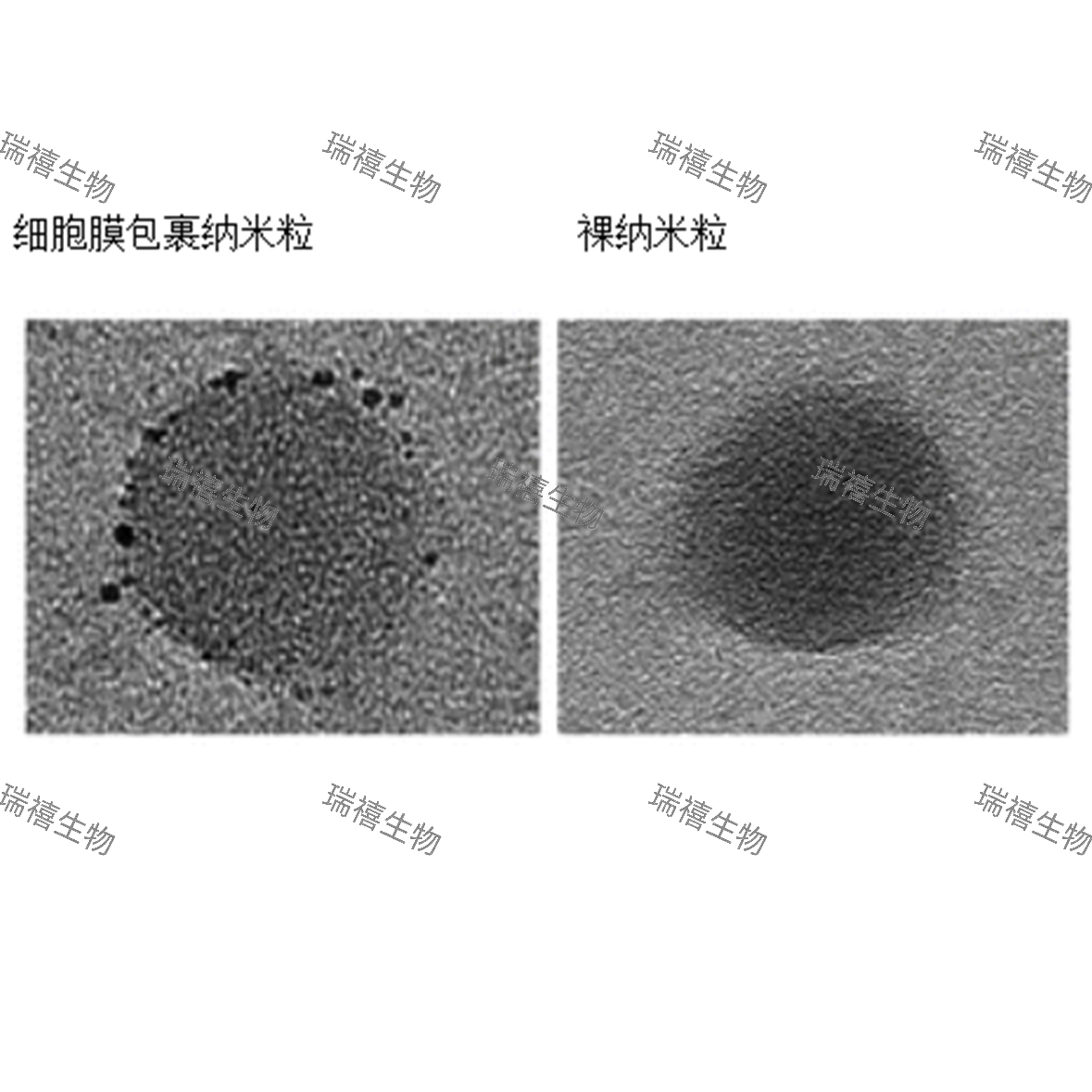
传统纳米金标记方法往往需要数小时甚至过夜反应,且偶联效率受限于分子大小、等电点等因素。本试剂盒对于这些因素进行优化:
反应动力学优化:采用双功能交联剂与纳米金表面工程化设计,将反应速率提升10倍以上,30分钟内即可完成偶联;
空间位阻消除技术:通过引入柔性间隔臂(如PEG链),降低纳米金与生物分子间的空间位阻效应,使偶联效率突破70%大关;
智能缓冲体系:内置pH缓冲系统可实时调节反应微环境,确保不同分子量蛋白(5-200 kDa)均能实现偶联。
作为真正的通用型试剂盒,其应用范围涵盖:
抗体类:单克隆抗体、多克隆抗体、Fab片段、scFv等;
蛋白类:酶(如HRP、AP)、细胞因子、受体蛋白、转录因子等;
多肽类:抗原表位肽、细胞穿透肽、环肽等;
核酸适配体:经氨基修饰的核酸分子亦可兼容。
通过验证实验表明,试剂盒对不同分子量(10 kDa-150 kDa)、等电点(pI 4.5-9.5)的生物分子均表现出良好的偶联性能,尤其对传统方法难以标记的小分子量蛋白(<30 kDa)效果好。
试剂盒采用"一管式"操作模式,仅需三步即可完成偶联:
活化阶段:将纳米金溶液与交联剂混合,室温孵育5分钟;
偶联阶段:加入抗体/蛋白溶液,37℃振荡反应25分钟;
纯化阶段:通过超滤离心(10 kDa MWCO)去除未反应试剂,获得高纯度偶联产物。
全程无需特殊设备,普通实验室条件下即可完成,特别适合高通量筛选与临床样本即时检测场景。

 2025-05-07 作者:wff 来源:
2025-05-07 作者:wff 来源:

