全氟己烯脂质体(Perfluorohexene Liposomes)是一种将全氟己烯(Perfluorohexene,C₆F₁₂)包裹于脂质双分子层结构中的纳米载体,结合了全氟化碳化合物的独特理化性质与脂质体的生物相容性,在药物递送、医学成像等领域展现出重要应用潜力。
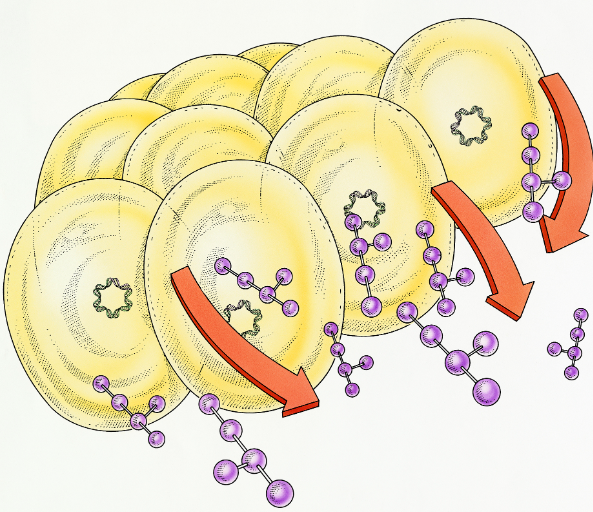
核心成分与功能
全氟己烯:作为全氟化碳化合物,具有高氧溶解度、低表面张力和化学惰性,可稳定携带氧气或药物分子。
脂质体载体:由磷脂双分子层构成,生物相容性良好,可保护内部全氟己烯免受降解,并实现靶向递送。
粒径控制:通过薄膜分散法、逆向蒸发法等制备技术,可调控脂质体粒径至纳米级(通常100-500nm),优化其在体内循环中的稳定性与穿透性。
表面修饰与功能化
脂质体表面可引入聚乙二醇(PEG)链、抗体或配体,延长循环时间、减少免疫清除,并实现特定部位的靶向富集。
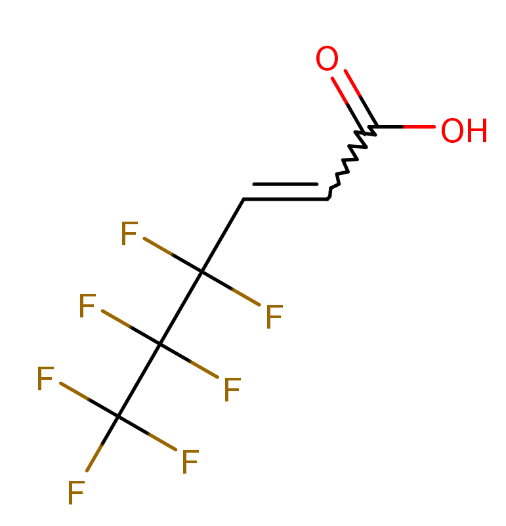
以下为定制过程中需重点考虑的技术要点:
一、核心材料与结构优化
脂质体成分
磷脂选择:采用进口高分子脂质材料构建双分子层结构,需确保其对全氟己烯的包封效率。例如,可通过调节磷脂链长(如DSPC、DPPC)与胆固醇比例,提升脂质体膜的稳定性。
全氟己烯特性:全氟己烯作为全氟化碳类物质,具有高氧溶解度与低表面张力,但需通过脂质体包裹降低其直接暴露风险。定制时需明确其纯度(如95%+)及分子稳定性。
粒径与表面修饰
粒径控制:根据应用场景调整粒径(如100-1000nm)。例如,超声成像需粒径小于1μm以增强穿透性,而药物递送可能需更大粒径以延长循环时间。
表面功能化:引入PEG链可减少免疫清除,延长半衰期;若需靶向递送,可偶联抗体(如抗HER2抗体)或配体(如RGD肽),实现靶向富集。
二、制备工艺定制
制备方法选择
薄膜分散法:适用于实验室小规模制备,通过将磷脂、胆固醇及全氟己烯溶于有机溶剂,减压蒸发形成薄膜后水化,可制备多层脂质体。
逆向蒸发法:将磷脂溶于有机溶剂,加入含全氟己烯的水相乳化后减压蒸发,适合高包封率需求,但需优化超声参数以避免全氟己烯挥发。
微流控技术:通过控制流速与混合比例,可制备粒径均一的单层脂质体,适合规模化生产。
纯化与后处理
挤出与超滤:通过聚碳酸酯膜(如100nm孔径)挤出可减小粒径并提高均一性;超滤可去除未包封的全氟己烯与有机溶剂残留。
冻干保护剂:若需长期储存,可添加蔗糖、海藻糖等冻干保护剂,防止脂质体聚集或融合。
三、质量控制与表征
关键指标检测
包封率:通过高效液相色谱(HPLC)或气相色谱(GC)测定全氟己烯的包封率,目标值需≥80%。
粒径与Zeta电位:使用动态光散射(DLS)检测粒径分布,目标PDI<0.3;Zeta电位(如-10mV)可反映脂质体稳定性。
全氟己烯含量:通过核磁共振(NMR)或质谱(MS)确认全氟己烯的化学结构与纯度。
稳定性评估
短期稳定性:在2-8℃下储存3个月,检测粒径、包封率及全氟己烯泄漏率。
长期稳定性:在-20℃下储存1年,评估脂质体的物理与化学稳定性。
四、应用场景适配
超声成像增强剂
需优化脂质体粒径至200-500nm,增强超声回波信号;表面修饰可引入靶向基团(如VEGFR抗体),实现靶向成像。
药物递送系统
若需共递送药物(如Chemotherapy 药),需通过pH敏感脂质体或光响应脂质体实现控制释放;需验证药物与全氟己烯的相容性。

 2025-05-08 作者:wff 来源:
2025-05-08 作者:wff 来源:

