聚酰胺-胺(PAMAM)树状大分子因其高度支化的三维结构、丰富的表面官能团及可调控的物理化学性质,成为纳米医学领域的重要载体。其定制化设计需从分子结构出发,通过功能模块的组装,实现药物递送及智能响应等多样化应用。
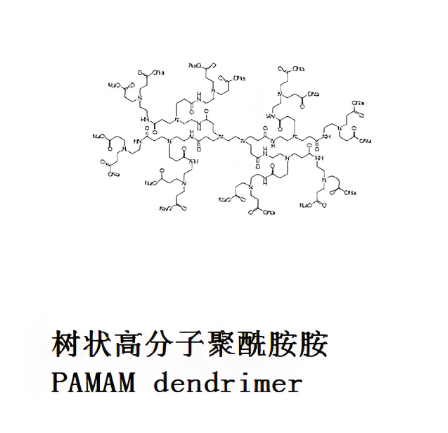
PAMAM分子结构的基本特征
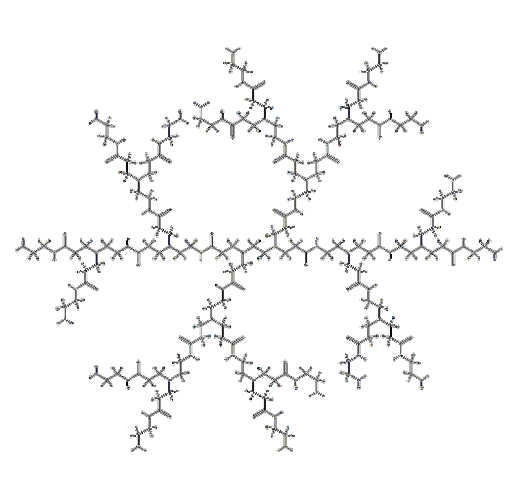
PAMAM纳米系统的核心是其高度分支的聚酰胺-胺结构。这种结构由中心核、分支单元和末端基团组成,其代数(G)决定了分子的大小和复杂性。低代数(如G0-G2)的PAMAM纳米系统具有较小的尺寸和较低的复杂性,而高代数(如G4-G6)则具有更大的尺寸和更高的分支程度。通过选择不同的中心核和末端基团,可以调节PAMAM纳米系统的物理化学性质,如溶解性、电荷和亲疏水性。
装载能力:内部空腔可高效包载DNA、siRNA等核酸药物,表面氨基通过静电作用与核酸结合,形成稳定的纳米复合物。
智能递送机制:阳离子表面助力复合物穿透细胞膜,树枝状结构通过“质子海绵效应”缓冲内体酸性环境,促进基因释放并进入细胞核。
功能化修饰潜力:表面氨基可偶联靶向配体(如叶酸、抗体)、PEG链或荧光探针,实现靶向递送与体内追踪。
PAMAM分子结构的定制化策略
中心核的选择:中心核的化学性质直接影响PAMAM纳米系统的整体结构和功能。常见的中心核包括氨、乙二胺和丙三胺等。通过选择不同的中心核,可以调节纳米系统的尺寸和稳定性。
末端基团的修饰:末端基团的化学性质决定了PAMAM纳米系统的表面性质和功能。常见的末端基团包括氨基、羧基、羟基和巯基等。通过化学修饰,可以引入特定的功能基团,如药物分子、荧光探针或靶向配体。
分支单元的调控:分支单元的数量和长度可以通过合成条件进行调控。通过调整合成过程中的反应时间和温度,可以实现对分支单元的控制,从而调节纳米系统的尺寸和结构。
PAMAM功能模块的构建
药物传递模块
PAMAM纳米系统在药物传递中的应用主要依赖于其能够与药物分子形成稳定的复合物。通过化学键合或物理包载,药物分子可以被固定在PAMAM纳米系统的内部或表面。为了提高药物传递的效率和靶向性,通常需要对PAMAM纳米系统进行表面修饰,引入靶向配体(如抗体、肽段或小分子配体)以实现对特定细胞或组织的靶向。
药物包载方法:包括共价键合、静电吸附和物理包载等。共价键合通过化学反应将药物分子固定在PAMAM纳米系统上,具有较高的稳定性和可控性;静电吸附则利用PAMAM纳米系统的表面电荷与药物分子之间的静电相互作用实现包载;物理包载则是将药物分子包载在PAMAM纳米系统的内部空腔中,适合于疏水性药物。
靶向配体的引入:通过化学修饰将靶向配体连接到PAMAM纳米系统的表面,可以实现对特定细胞或组织的靶向。例如,将叶酸连接到PAMAM纳米系统表面可以实现对特定细胞的靶向,因为Cancer细胞表面高表达叶酸受体。
生物成像模块
PAMAM纳米系统在生物成像中的应用主要依赖于其能够与荧光探针或磁性材料结合,形成具有成像功能的纳米探针。通过化学修饰,可以将荧光探针或磁性材料固定在PAMAM纳米系统的表面或内部,从而实现对生物组织或细胞的成像。
荧光探针的引入:通过化学修饰将荧光探针连接到PAMAM纳米系统的表面或内部,可以实现对生物组织或细胞的荧光成像。荧光探针的选择取决于成像的需求,如荧光强度、发射波长和光稳定性等。
磁性材料的引入:通过化学修饰将磁性材料(如铁氧化物纳米颗粒)固定在PAMAM纳米系统的表面或内部,可以实现对生物组织或细胞的磁共振成像(MRI)。磁性材料的选择取决于成像的需求,如磁性强度和生物相容性等。
PAMAM纳米系统的定制化设计从分子结构到功能模块的构建,为其实现多种应用提供了强大的工具。通过调控分子结构和功能模块,可以实现PAMAM纳米系统在药物传递、生物成像等领域的应用。

 2025-07-15 作者:wff 来源:
2025-07-15 作者:wff 来源:

