氨甲基化反应是有机合成化学中一种重要的反应类型,能够将氨甲基基团引入到目标分子中,为合成具有生物活性的化合物、功能材料等提供关键步骤。在氨甲基化反应过程中,溶剂扮演着至关重要的角色,它可以影响反应的速率、选择性和反应机理。因此,深入研究溶剂效应对氨甲基化反应机理的影响具有重要的理论和实际意义。
一、氨甲基化反应概述
氨甲基化反应通常涉及到含有活性氢的底物、氨甲基化试剂以及催化剂等。常见的氨甲基化试剂包括甲醛和胺的缩合物等。反应过程中,底物的活性氢被氨甲基取代,形成新的 C - N 键。根据底物和反应条件的不同,氨甲基化反应可以通过多种途径进行,如亲核取代、加成等反应机理。
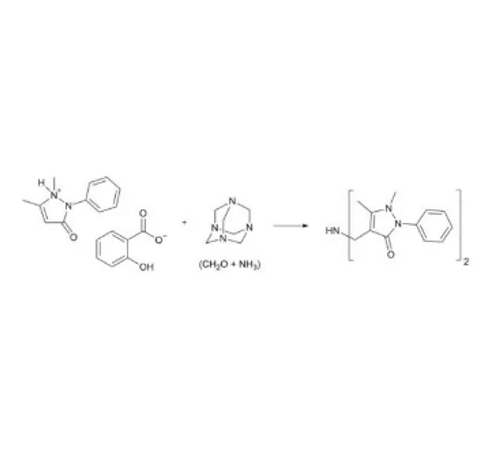
二、溶剂效应的影响因素
(一)溶剂的极性
溶剂的极性对氨甲基化反应机理有着深刻的影响。在极性较强的溶剂中,反应物和中间体的电荷分布更容易被溶剂分子所稳定。例如,对于亲核型的氨甲基化反应,极性溶剂可以促进亲核试剂的解离和稳定中间体的电荷。相反,在非极性溶剂中,反应可能更倾向于通过非极性相互作用主导的途径进行,如形成氢键或范德华力较弱的中间体。
(二)溶剂的氢键能力
如果溶剂具有较强的氢键形成能力,它可以与反应物、中间体或产物形成氢键。在氨甲基化反应中,这可能会改变反应中间体的稳定性和反应活性。例如,当溶剂能够与氨甲基化试剂中的氨基形成氢键时,可能会影响氨基的亲核性,从而改变反应速率和选择性。对于某些含有羟基或羰基等官能团的底物,溶剂与这些官能团形成的氢键可能会改变底物的活性位点暴露程度,进而影响反应的进行。
(三)溶剂的离子化能力
对于一些在反应过程中会产生离子中间体的氨甲基化反应,溶剂的离子化能力至关重要。良好的离子化溶剂能够促进离子中间体的形成和稳定,降低反应的活化能。例如,在使用金属盐作为催化剂的氨甲基化反应中,溶剂对金属离子的溶剂化作用会影响金属离子与反应物之间的相互作用,从而改变反应机理。
三、溶剂效应在反应机理中的具体体现
(一)对反应速率的影响
合适的溶剂可以提高氨甲基化反应的速率。通过稳定反应中间体,溶剂能够降低反应的活化能。例如,在某些极性溶剂中,氨甲基化反应的速率常数比在非极性溶剂中高出数倍。这是因为极性溶剂有利于亲核试剂的进攻和中间体的形成,加速了反应的进行。
(二)对反应选择性的影响
溶剂还可以影响氨甲基化反应的选择性。在不同的溶剂中,反应可能会朝着生成不同产物的方向进行。这是由于溶剂对不同反应途径的中间体稳定性影响不同。例如,在一种溶剂中可能有利于生成单氨甲基化产物,而在另一种溶剂中可能更倾向于生成多氨甲基化产物,这取决于溶剂对不同反应中间体的稳定作用。
溶剂效应在氨甲基化反应机理中具有不可忽视的影响。溶剂的极性、氢键能力和离子化能力等因素通过改变反应物、中间体的稳定性和相互作用,对反应速率和选择性产生重要作用。深入理解溶剂效应有助于我们更好地设计氨甲基化反应条件,优化反应过程,提高目标产物的产率和选择性,为有机合成化学领域中氨甲基化反应的进一步发展和应用提供有力的理论支持。

 2025-02-12 作者:lkr 来源:
2025-02-12 作者:lkr 来源:

