PLGA-b-PEOz(聚乳酸-羟基乙酸共聚物-嵌段-聚2-乙基-2-噁唑啉)是一种两亲性嵌段共聚物,由疏水性的PLGA(聚乳酸-羟基乙酸共聚物)和亲水性的PEOz(聚2-乙基-2-噁唑啉)通过化学键连接而成。这种材料结合了PLGA的生物可降解性和PEOz的独特物理化学性质(如温敏性、低免疫原性),在药物递送、纳米医学和生物材料领域展现出广阔的应用前景。
一、载体结构与药物负载的适配性优势
双极性负载能力,适配多类型药物
PLGA 的疏水性核心可高效包裹脂溶性药物(如紫杉醇、姜黄素),负载率通常达 10%-20%;
PEOz 的亲水性链段可通过氢键或静电作用结合水溶性药物(如小分子抑制剂、多肽),解决传统 PLGA 对亲水性药物负载率低(<5%)的问题,扩展了可负载药物的范围。
例如:对水溶性Chemotherapy 药物顺铂,PLGA-b-PEOz 的负载率(15%)明显高于纯 PLGA(5%),且药物分散更均匀。
稳定的胶束结构,减少药物提前泄露
在水溶液中自组装形成核-壳型胶束(PLGA 为核,PEOz 为壳),临界胶束浓度(CMC)低(通常 1-50 μg/mL),在稀释的生理环境中不易解聚,避免药物在血液循环中提前释放(突释率可控制在 < 10%)。
相比 PLGA-PEG 共聚物,PEOz 的空间位阻更强,胶束结构更稳定,在血清中放置 48 小时后粒径变化 < 10%(PLGA-PEG 胶束变化达 30%)。
二、药物释放的可控性与长效性优势
双机制协同释放,实现准确调控
药物释放同时依赖 PLGA 的水解降解和药物在载体中的扩散:
初期:少量药物通过 PEOz 壳层的扩散缓慢释放(避免暴释Poison 性);
中期:随 PLGA 核的逐步降解,药物持续释放(主要阶段,可持续 2-8 周);
后期:PLGA 完全降解,剩余药物释放完毕。
通过调节 PLGA 的 LA/GA 比例(如 50:50 降解快于 75:25)或 PEOz 分子量(如 5kDa PEOz 比 2kDa 更易阻碍扩散),可准确调控释放速率(如从每天释放 1% 至 5% 可调)。
酸性微环境缓冲,保护药物活性
PLGA 降解产生乳酸和羟基乙酸,可能导致局部酸性环境(pH 降至 5.0-6.0),破坏敏感药物(如蛋白、疫苗)的活性。
PEOz 具有弱碱性(pKa≈7.5),可中和部分酸性产物,维持载体内部 pH 稳定(pH 6.5-7.0),明显提高蛋白类药物的缓释稳定性(如胰岛素在 PLGA-b-PEOz 中 30 天活性保留率达 80%,纯 PLGA 中仅 50%)。
三、生物相容性与体内行为的优势
低Poison 性与低免疫原性,提升生物安全性
PLGA 降解产物为人体代谢物,无长期Poison 性;PEOz 的化学结构类似天然多肽,生物相容性良好,对细胞的Poison 性(IC₅₀>500 μg/mL)明显低于 PEG(部分 PEG 衍生物可能引发抗体反应)。
体内实验显示,PLGA-b-PEOz 胶束静脉注射后,小鼠血清中Inflammation因子(IL-6、TNF-α)水平与生理盐水组无明显差异,远低于 PLGA-PEG 组(Inflammation因子水平升高 2-3 倍)。
延长循环时间,提高病灶富集
PEOz 链在胶束表面形成水化层,其 “隐身” 效果优于 PEG:可减少单核-巨噬细胞系统的吞噬,延长体内半衰期(t₁/₂≈12 小时,PLGA-PEG 为 6 小时)。
通过tumourBlood vessels的高通透性和滞留效应(EPR 效应),PLGA-b-PEOz 载药系统在tumour部位的蓄积量是游离药物的 10-15 倍,明显提高局部药物浓度。
名称:PLGA-b-PEOz
产品规格:mg/g
纯度:95%+
保存方式:-20℃以下,避光,防潮
保质期限:12个月
用途:科研
温馨提示:仅用于科研,不能用于人体
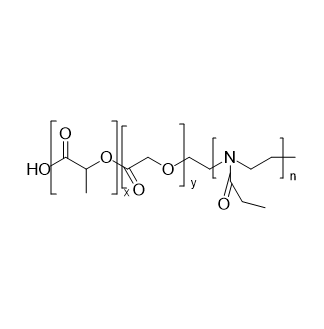
图:PLGA-b-PEOz

 2025-08-12 作者:ws 来源:
2025-08-12 作者:ws 来源:

