谷胱甘肽修饰的金纳米颗粒(GSH-AuNPs)是通过谷胱甘肽(Glutathione,GSH,一种三肽,序列为 γ-Glu-Cys-Gly) 修饰金纳米颗粒(AuNPs)形成的功能性纳米复合材料。
一、优化配体层结构与修饰密度
GSH-AuNPs 的稳定性核心依赖于表面配体层的致密性和相互作用强度,通过调控配体修饰方式可明显提升稳定性。
提高 GSH 修饰密度
原理:增加单位面积 GSH 分子数量,通过更强的空间位阻和静电排斥抑制颗粒团聚。
方法:制备时提高 GSH 与金的摩尔比,或延长配体交换时间,确保 AuNPs 表面被 GSH 充分覆盖。
效果:修饰密度从 2 个分子/nm² 提升至 5 个分子/nm² 以上时,在 0.5 M NaCl 溶液中的团聚率可降低 50% 以上。
引入辅助配体协同修饰
亲水性高分子配体:将 GSH 与聚乙二醇巯基(PEG-SH)共修饰,PEG 链(如分子量 2000 Da)的长链空间位阻可增强抗盐性和抗蛋白质吸附能力。例如,GSH:PEG-SH=3:1 共修饰的 AuNPs,在 10% 血清中可稳定 72 小时(纯 GSH 修饰仅稳定 24 小时)。
双巯基配体:加入少量双巯基化合物(如 1,6-己二硫醇),通过 “桥联” 作用将相邻 GSH 分子交联,增强配体层与 AuNPs 表面的结合力,减少 GSH 脱落(尤其在酸性条件下)。
配体末端功能化修饰
对 GSH 的羧基进行甲基化或 PEG 化修饰,减少分子间氢键导致的配体层收缩,同时增强与水的相互作用,提升在有机溶剂-水混合体系中的稳定性。
二、构建核-壳或复合结构
通过在 GSH-AuNPs 表面包覆惰性材料,形成物理屏障隔绝外界干扰,适用于极端环境(如强酸、高离子强度)。
包覆二氧化硅(SiO₂)壳层
方法:在 GSH-AuNPs 溶液中加入正硅酸乙酯(TEOS),在氨水催化下发生溶胶-凝胶反应,形成 5-20 nm 的 SiO₂壳层。
优势:SiO₂化学惰性强,可耐受 pH 2-12 的极端条件,且不影响 GSH 的生物活性(如与金属离子的结合能力)。例如,GSH-AuNPs@SiO₂在 1 M HCl 中浸泡 24 小时后,SPR 峰偏移量 <5 nm(纯 GSH-AuNPs 偏移> 30 nm)。
组装金属有机框架(MOFs)外壳
方法:利用 GSH 的羧基与金属离子(如 Zn²⁺、Cu²⁺)的配位作用,在表面原位生长 MOFs(如 ZIF-8),形成多孔保护壳。
优势:MOFs 外壳不仅增强稳定性,还可负载药物,实现 “保护-递送” 一体化。例如,ZIF-8 包覆的 GSH-AuNPs 在含蛋白酶的血清中,GSH 保留率从 30% 提升至 80%。
形成聚合物网络涂层
通过光聚合或热聚合在 GSH-AuNPs 表面交联聚乙二醇二丙烯酸酯(PEGDA),形成水凝胶网络,提升机械稳定性和抗剪切能力,适用于流动体系(如微流控芯片)。
三、调控环境适配性
针对 GSH-AuNPs 应用场景的环境特征(如 pH、温度、生物介质),通过预处理或化学修饰增强适配性。
pH 响应性优化
酸性环境稳定化:在 GSH 中混入少量含咪唑基的巯基配体(如巯基咪唑),酸性条件下咪唑质子化产生正电排斥,抵消 GSH 羧基质子化导致的电荷减弱。例如,在 pH 4.0 时,混合修饰的 AuNPs 团聚率比纯 GSH 修饰降低 60%。
碱性环境稳定化:加入少量巯基乙胺(带氨基),碱性条件下氨基去质子化增强负电荷,维持静电排斥。
抗生物 fouling 修饰
生物体系中的蛋白质、核酸易吸附于 GSH-AuNPs 表面导致团聚,可通过以下方式改善:
共修饰牛血清白蛋白(BSA),利用 BSA 的空间位阻屏蔽 AuNPs 表面,减少非特异性吸附;
表面接枝聚(甲基丙烯酸寡聚乙二醇酯)(POEGMA),其抗蛋白质吸附性能优于 PEG,可使 AuNPs 在 50% 血清中稳定 5 天以上。
温度稳定性提升
对 GSH-AuNPs 进行低温预处理(如 4℃孵育 24 小时),促进配体层有序排列;或加入少量糖分子(如蔗糖、海藻糖),通过氢键稳定水合层,使 AuNPs 在-20℃冷冻-解冻循环中保持分散。
名称:谷胱甘肽修饰的金纳米颗粒
产品规格:mg/g
纯度:95%+
保存方式:-20℃以下,避光,防潮
保质期限:12个月
用途:科研
温馨提示:仅用于科研,不能用于人体
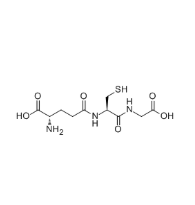
图:谷胱甘肽

 2025-08-18 作者:ws 来源:
2025-08-18 作者:ws 来源:

