在生物医药领域,纳米粒子作为药物递送载体备受关注。PEG-PCL-PEA(聚乙二醇-聚己内酯-聚酯酰胺)因其独特结构和性能,成为构建纳米粒子的理想材料。
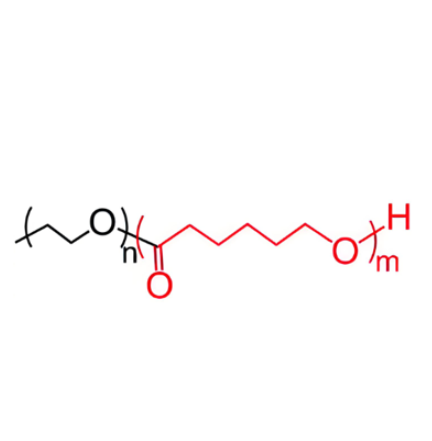
图为:PEG-PCL-PEA结构式
PEG-PCL-PEA 纳米粒子常采用纳米沉淀法制备。首先,将 PEG-PCL-PEA 共聚物溶解于与水互溶的有机溶剂,如丙酮或四氢呋喃中,形成均匀溶液。药物若为疏水性,可同时溶于该有机相;若为亲水性药物,后续需特殊处理。接着,在搅拌下将上述溶液缓慢滴加到大量水相中。由于有机溶剂快速扩散至水相,导致 PEG-PCL-PEA 共聚物溶解度急剧下降,进而自组装形成纳米粒子。持续搅拌一段时间,使纳米粒子结构稳定后,通过旋转蒸发或透析等方式去除有机溶剂。最后,经离心、冷冻干燥等操作,获得 PEG-PCL-PEA 纳米粒子粉末。
制备的纳米粒子呈现出特殊特性。粒径方面,通过调节共聚物浓度、有机相与水相比例以及搅拌速度等条件,可将纳米粒子粒径准确控制在几十到几百纳米。例如,提高共聚物浓度,纳米粒子粒径会增大;加快搅拌速度,粒径则减小。形态上,借助透射电子显微镜(TEM)观察,纳米粒子多呈规则球形,分散较为均匀,这为其在体内均匀分布及发挥作用奠定基础。
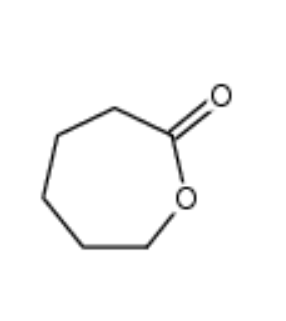
图为:聚己内酯结构式
从性能特性看,PEG-PCL-PEA 纳米粒子的生物相容性良好。PEG 链段赋予纳米粒子亲水性,降低蛋白质非特异性吸附,减少免疫系统识别与清除,延长其在血液循环中的时间。PEA 中的酰胺键增强分子间作用力,使纳米粒子结构更稳定,且其良好的生物降解性,让纳米粒子在完成药物递送使命后,可逐渐分解为小分子排出体外,减少体内残留风险。在药物负载与释放上,疏水性 PCL 和 PEA 内核为疏水性药物提供存储空间,亲水性 PEG 外壳利于亲水性药物附着或包裹。体外药物释放实验显示,纳米粒子可实现药物的缓慢释放,在不同 pH 值和酶环境下,释放速率有所差异。如在模拟tumor微酸性环境中,由于 PEA 中酯键水解加快,药物释放速率会提升,有助于提高tumor部位药物浓度,增强Treatment 效果。

 2025-08-20 作者:lkr 来源:
2025-08-20 作者:lkr 来源:

