叶酸-聚乙二醇-叠氮作为一种多功能生物分子,在靶向药物递送和生物医学成像中展现出巨大潜力。其核心作用机制在于其能够与细胞表面的叶酸受体发生特异性结合,从而实现对特定细胞的靶向递送和成像。
一、FA-PEG-N3的分子结构特性
FA-PEG-N3由叶酸(FA)、聚乙二醇(PEG)和叠氮基团(N3)三部分组成。叶酸作为维生素B族衍生物,能够特异性地与细胞表面的叶酸受体结合。聚乙二醇部分则提供了良好的水溶性和生物相容性,使得FA-PEG-N3在生物体内更稳定,减少immunity反应。叠氮基团则赋予FA-PEG-N3高反应性,能够参与点击化学反应,与其他分子进行偶联。
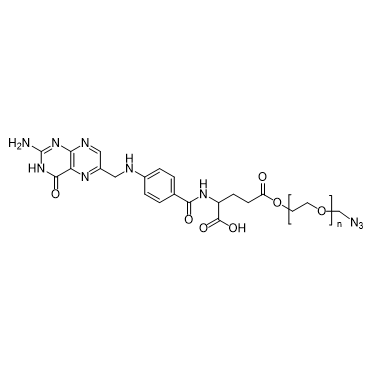
图为:FA-PEG-N3结构式
二、与叶酸受体的相互作用机制
叶酸受体在多种tumor细胞表面高表达,而在正常细胞表面表达较低。FA-PEG-N3中的叶酸部分能够与叶酸受体发生特异性结合,这种结合具有高亲和力和选择性。结合后,FA-PEG-N3通过受体介导的内吞作用进入细胞,从而实现靶向递送。
三、分子机制的具体过程
识别与结合:FA-PEG-N3的叶酸部分首先识别并结合到细胞表面的叶酸受体上,形成稳定的复合物。
内吞作用:复合物通过受体介导的内吞作用进入细胞,形成内涵体。
内涵体逃逸:在内涵体酸性环境下,FA-PEG-N3可能通过某种机制(如PEG链的质子海绵效应)促进内涵体膜破裂,释放出所包裹的药物或成像分子。
靶向递送:释放出的药物或成像分子在细胞内发挥作用,实现靶向Treatment 或成像。
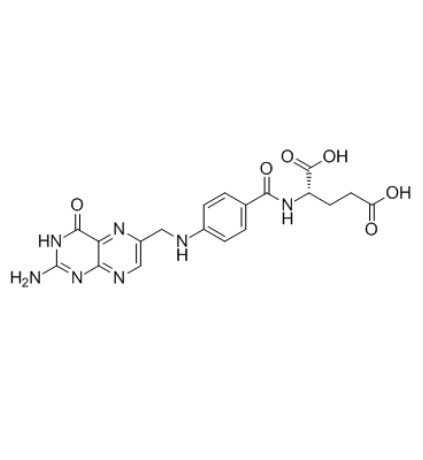
图为:叶酸结构式
四、影响因素与优化策略
FA-PEG-N3与叶酸受体的相互作用受多种因素影响,包括叶酸受体的表达水平、FA-PEG-N3的浓度和分子量等。通过优化FA-PEG-N3的分子量、叶酸与PEG的比例以及叠氮基团的反应活性,可以提高其与叶酸受体的结合效率和靶向递送能力。
五、应用前景
FA-PEG-N3与细胞表面叶酸受体的相互作用机制为靶向药物递送和生物医学成像提供了新的思路。未来,通过进一步研究其分子机制和优化合成工艺,FA-PEG-N3有望在tumorTreatment 、疾病诊断等领域发挥更大的作用。同时,结合点击化学技术,FA-PEG-N3还可以与其他功能分子进行偶联,构建出具有更复杂功能的生物材料。

 2025-06-05 作者:lkr 来源:
2025-06-05 作者:lkr 来源:

