DSPE-DDP(1,2-二硬脂酰-sn-甘油-3-磷酸乙醇胺-顺铂)作为一种新型磷脂衍生物,在脂质体药物递送系统中展现出优势,其通过化学修饰将顺铂(DDP)与磷脂分子结合,影响了脂质体的稳定性和靶向性。
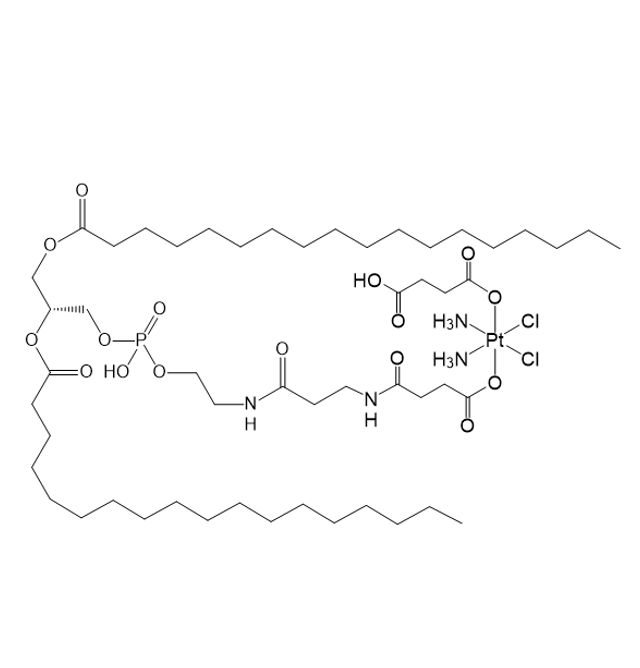
图为:DSPE-DDP结构式
一、对脂质体稳定性的影响
DSPE-DDP的引入提升了脂质体的物理和化学稳定性。DSPE作为磷脂分子,具有较高的熔点和双分子层结构稳定性,能够抵抗体内环境的降解。顺铂的偶联进一步增强了脂质体的稳定性,减少药物在blood循环中的泄漏。例如,DSPE-DDP修饰的脂质体在体外实验中表现出更长的半衰期和更低的非特异性吸附,这得益于DSPE的硬脂酸链形成的紧密双分子层结构以及顺铂与磷脂的共价结合。此外,DSPE-DDP的引入还减少了脂质体与plasma蛋白的非特异性相互作用,降低了被网状内皮系统(RES)快速清除的风险,从而延长了脂质体在体内的循环时间。
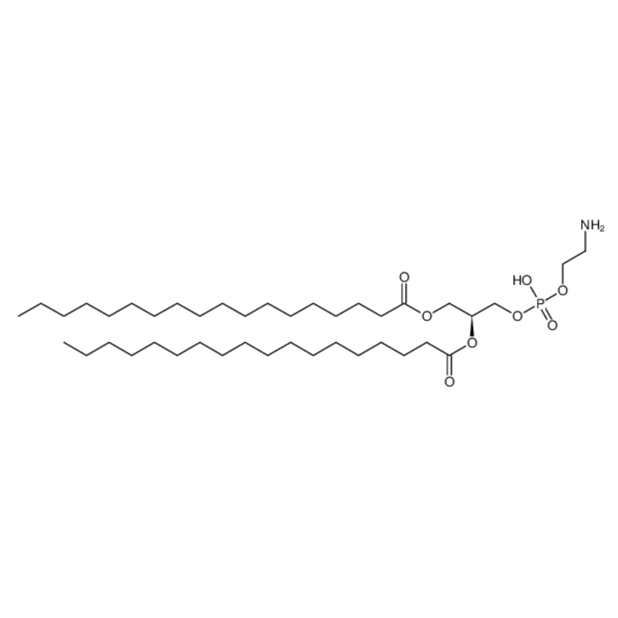
图为:DSPE结构式
二、对脂质体靶向性的影响
DSPE-DDP通过顺铂的化学修饰,赋予了脂质体一定的靶向性。顺铂作为一种Chemotherapy 药物,对tumor细胞具有高有害性,但其靶向性较差。通过DSPE-DDP的构建,顺铂被限制在脂质体内部,减少了在正常组织中的分布,从而提高了对tumor细胞的靶向性。此外,DSPE-DDP还可以与其他靶向分子(如抗体、多肽)结合,进一步增强脂质体的靶向性。例如,将DSPE-DDP与叶酸(FA)结合,可以构建叶酸受体靶向的脂质体,实现对叶酸受体高表达的tumor细胞的准确递送。这种靶向性不仅提高了药物的Therapeutic effect ,还减少了副作用。
三、应用前景与挑战
DSPE-DDP修饰的脂质体在tumorTreatment 中展现出巨大潜力,其通过提高稳定性和靶向性,实现了药物的高效递送和低有害性。然而,仍需关注其长期有害性和体内代谢机制,以确保临床应用的安全性。未来,通过进一步优化DSPE-DDP的合成工艺和表面修饰,可实现更高效、更稳定的脂质体药物递送系统。

 2025-06-05 作者:lkr 来源:
2025-06-05 作者:lkr 来源:

