在生物医学和生物技术领域,蛋白质固定化技术对于提升蛋白质的稳定性、可重复利用性以及准确调控其功能至关重要。其中,基于 Galactose-PEG-NH₂(半乳糖-聚乙二醇-氨基)的蛋白质固定化技术正逐渐崭露头角,展现出独特优势。
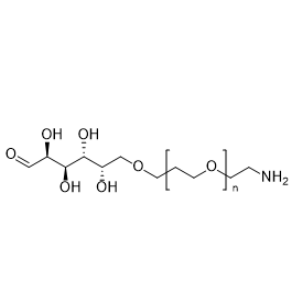
图为:Galactose-PEG-NH₂结构式
Galactose-PEG-NH₂由三部分构成。半乳糖(Galactose)具有良好的生物亲和性,能够特异性地与某些细胞表面受体或生物分子相互作用,为固定化蛋白质提供了潜在的靶向性。聚乙二醇(PEG)则是一种亲水性聚合物,它赋予了整个分子良好的水溶性和稳定性,可有效减少蛋白质在固定化过程中的聚集与变性,并且降低其immunity原性,使固定化后的蛋白质在生物体内或复杂环境中更易保持活性。而末端的氨基(NH₂)作为活性基团,是实现蛋白质共价连接的关键位点。
利用 Galactose-PEG-NH₂进行蛋白质固定化,主要通过氨基与蛋白质分子上的羧基、醛基等官能团发生化学反应,形成稳定的共价键。这一过程通常在温和的条件下进行,如合适的 pH 值和温度范围,以最大程度减少对蛋白质天然结构和活性的影响。例如,在一定 pH 值的缓冲溶液中,将 Galactose-PEG-NH₂与目标蛋白质混合,通过缩合剂(如碳化二亚胺类试剂)的作用,促使氨基与蛋白质羧基脱水缩合,实现蛋白质的固定化。
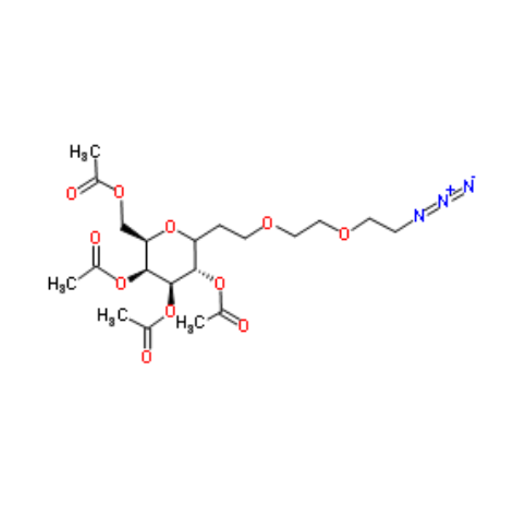
图为:半乳糖结构式
这种固定化技术在多个领域有着应用。在生物传感器的构建中,将特定的识别蛋白(如抗体、酶等)通过 Galactose-PEG-NH₂固定在传感器表面,利用半乳糖的靶向性可提高传感器对目标分析物的识别能力,PEG 的稳定作用能确保蛋白质在长期使用中保持活性,从而提升传感器的灵敏度和稳定性。在药物递送系统里,固定化的蛋白质药物可以借助 Galactose-PEG-NH₂的特性,实现对特定细胞或组织的靶向递送,同时 PEG 链能够延长药物在体内的循环时间,提高药物Therapeutic effect 。在工业酶催化过程中,基于 Galactose-PEG-NH₂固定化的酶能够方便地从反应体系中分离回收,多次重复使用,降低生产成本。
与传统蛋白质固定化方法相比,基于 Galactose-PEG-NH₂的技术优势明显。它不仅能有效维持蛋白质的活性,还引入了靶向功能和良好的生物相容性。不过,该技术也面临一些挑战,如合成 Galactose-PEG-NH₂的成本相对较高,固定化过程的反应条件需要准确控制以保证均一性等。但随着研究的深入和技术的不断改进,基于 Galactose-PEG-NH₂的蛋白质固定化技术有望在更多领域取得突破,为生物医学和生物技术的发展提供强大助力。

 2025-06-10 作者:lkr 来源:
2025-06-10 作者:lkr 来源:

