异硫氰酸荧光素-谷氨酰胺作为一种荧光标记物,其荧光光谱特性受溶剂极性与 pH 的影响,深入探究这些影响机制对优化其在生物分析、药物递送等领域的应用具有重要意义。
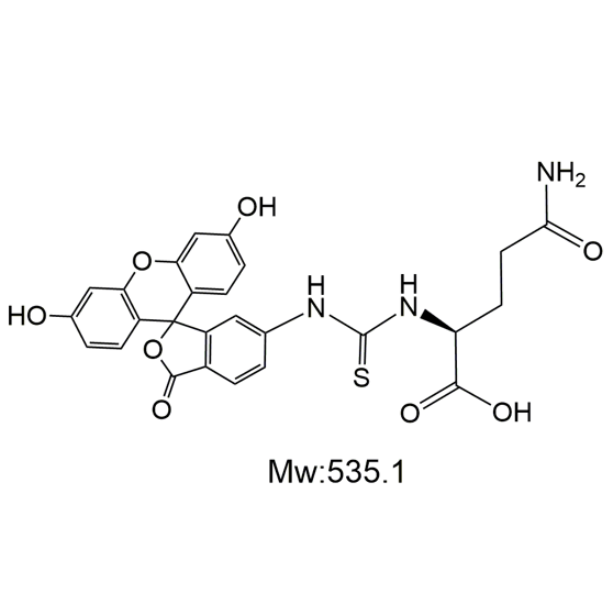
图为:FITC-Glutamine结构式
从溶剂极性来看,FITC-Glutamine 分子的荧光光谱呈现出明显的溶剂化效应。在极性溶剂如水中,FITC-Glutamine 的激发和发射光谱通常发生红移,这是由于极性溶剂分子与 FITC-Glutamine 分子间形成氢键或偶极-偶极相互作用,稳定了激发态分子,降低了激发态与基态之间的能级差,从而使荧光发射波长变长。相反,在非极性溶剂如环己烷中,缺乏这种稳定作用,光谱则表现为蓝移。例如,实验数据显示,FITC-Glutamine 在水中的最大发射波长约为 520 nm,而在环己烷中则蓝移至 505 nm 左右。
pH 对 FITC-Glutamine 荧光光谱的影响主要源于 FITC 分子中酚羟基的质子化与去质子化过程。在酸性环境下(pH <7),酚羟基保持质子化状态,此时荧光强度较弱;随着 pH 升高(pH> 7),酚羟基逐渐去质子化形成酚氧负离子,荧光强度增强。当 pH 达到 9-10 时,荧光强度达到峰值,继续升高 pH,由于分子结构的碱性降解,荧光强度又会逐渐下降。这一特性使得 FITC-Glutamine 可作为 pH 响应型荧光探针,用于监测细胞内或环境中的 pH 变化。
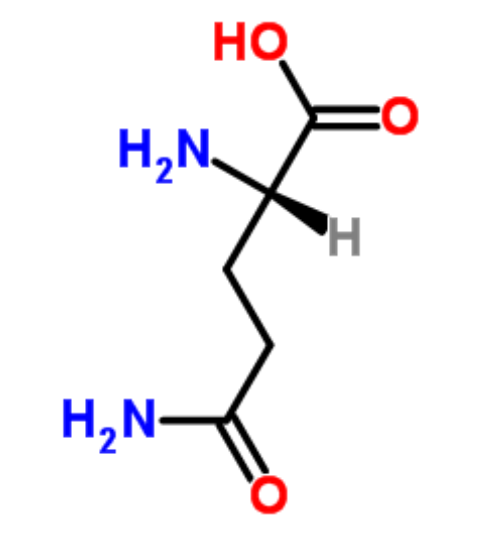
图为:谷氨酰胺结构式
通过系统研究 FITC-Glutamine 的荧光光谱与溶剂极性、pH 的依赖关系,不仅有助于理解其荧光变化的本质,还能为其在复杂生物体系或动态环境中的准确应用提供理论依据,进一步拓展其在生物传感、细胞成像等领域的应用边界。

 2025-07-02 作者:lkr 来源:
2025-07-02 作者:lkr 来源:

