N3-PEG-MAL 作为一种重要的异双活性基团 PEG 衍生物,在生物医学领域应用较广,其硫醚键形成动力学对生物标记有着重要影响。
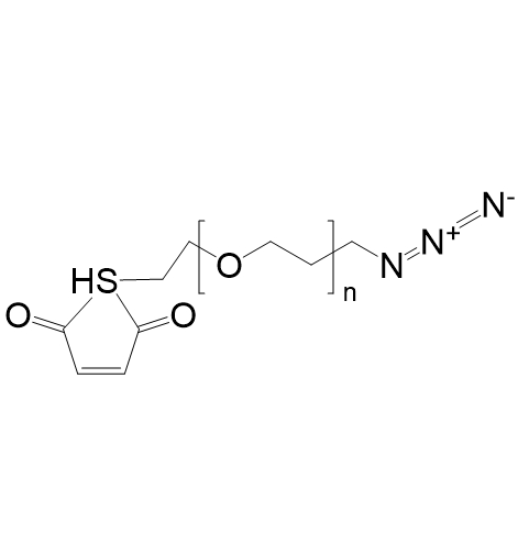
图为:N3-PEG-MAL结构式
N3-PEG-MAL 一端的叠氮基(N3)可参与点击化学反应,如与炔基在铜离子催化下高效反应,也能和 DBCO 直接反应,无需铜离子催化剂。另一端的马来酰亚胺(MAL)基团则具有高度特异性,在 pH 6.5-7.5 的温和条件下,能迅速与含巯基(-SH)的分子,如蛋白质半胱氨酸残基发生反应,形成稳定的硫醚键。PEG 链段赋予了分子良好的亲水性,不仅提升了修饰分子的溶解性,还能增强其生物相容性,减少多肽和蛋白质的免疫原性,同时抑制带电分子在修饰表面的非特异性结合。
在硫醚键形成动力学方面,MAL 与巯基的反应速率受多种因素调控。pH 值是关键因素之一,在 pH 6.5-7.5 时反应速率较快,这是因为在此 pH 区间,MAL 和巯基的活性较高,能有效促进反应进行。反应物浓度也影响明显,提高 MAL-PEG-N3 和含巯基分子的浓度,可加快反应进程,使硫醚键更快形成。此外,温度适当升高能增加分子热运动,加快反应速度,但过高温度可能导致分子结构变化,影响反应效果。
图为:马来酰亚胺结构式
在生物标记应用中,利用 N3-PEG-MAL 的硫醚键形成特性,可实现对生物分子的准确标记。例如在蛋白质标记中,通过 MAL 与蛋白质中的巯基结合,将叠氮基团引入蛋白质,后续再利用叠氮基的点击反应,连接上荧光染料等标记物,实现对蛋白质的可视化追踪,助力研究蛋白质在细胞内的定位、运输和相互作用等过程。在抗体药物偶联物(ADC)制备中,该物质可修饰抗体,先通过 MAL 与抗体的巯基形成硫醚键,再经点击反应连接药物分子,实现药物的靶向递送,提高Treatment 效果。

 2025-07-17 作者:lkr 来源:
2025-07-17 作者:lkr 来源:

