在生物医学与材料科学领域,PEG 衍生物因独特性能备受青睐。MPEG-SAS(甲氧基聚乙二醇琥珀酰胺琥珀酰亚胺酯)作为其中一员,与其他常见 PEG 衍生物相比,性能各有优劣。
从反应活性看,MPEG-SAS 的琥珀酰胺琥珀酰亚胺酯基团能与生物分子的氨基高效反应,形成稳定酰胺键。在蛋白质修饰中,可准确连接。对比 MPEG-VS(甲氧基聚乙二醇乙烯砜),后者虽也能与氨基反应,但对巯基的反应活性更高,且需在特定 pH 范围(7-9)才能与巯基快速反应生成硫醚键。在复杂生物体系,MPEG-VS 选择性反应优势明显,MPEG-SAS 在以氨基修饰为主的应用里表现突出。
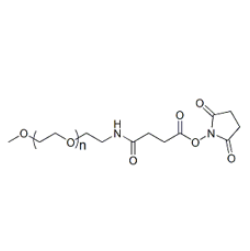
图为:MPEG-SAS结构式
稳定性方面,MPEG-SAS 具有优势。其 PEG 与 NHS 酯间的 C2 脂族酰胺键,使其水解半衰期长于部分含酯键的 PEG 衍生物。如 MPEG-SS(甲氧基聚乙二醇琥珀酰亚胺琥珀酸酯),与蛋白质赖氨酸偶合生成的产物中,MPEG 与 SS 连接的酯键易水解,产生免疫原性半抗原的 PEG;而 MPEG-SAS 结构稳定,可减少副反应。不过,相较于一些耐水解的 PEG 衍生物,如某些含醚键连接的两臂 PEG,MPEG-SAS 在极端条件下的稳定性稍逊一筹。
水溶性和生物相容性上,多数 PEG 衍生物都具备良好表现。MPEG-SAS 因 PEG 链段作用,能溶于水及多种有机溶剂,可降低蛋白质、细胞在材料表面吸附,减少免疫原性。多臂 PEG 虽亲水性强、生物相容性好,但因其支化结构,水溶性略低于线性的 MPEG-SAS。
在实际应用场景中,MPEG-SAS 常用于蛋白质、多肽等生物分子的修饰,提升其稳定性与循环半衰期;多臂 PEG 凭借高稳定性和独特结构,在靶向药物输送、组织工程支架构建方面更具优势;MPEG-VS 则因对巯基的高选择性,在抗体 / 蛋白修饰、构建 PEG 化药物载体时被应用。
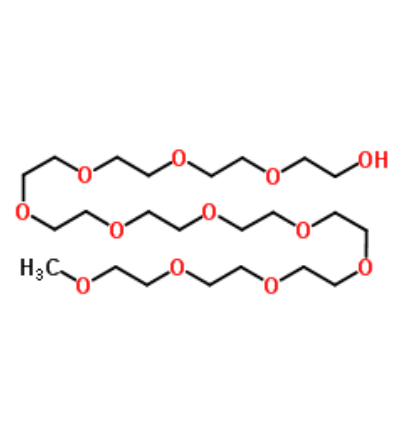
图为:MPEG结构式
总之,MPEG-SAS 与其他 PEG 衍生物各有性能特点。需依据具体应用需求,如反应对象、环境条件、预期效果等,合理选择 PEG 衍生物,以充分发挥其在生物医学、材料科学等领域的作用,推动相关技术发展。

 2025-08-20 作者:lkr 来源:
2025-08-20 作者:lkr 来源:

