PLGA纳米粒(100NM)负载GFP蛋白产品介绍:
PLGA纳米粒(100NM)负载GFP蛋白是一种基于聚乳酸-羟基乙酸共聚物(PLGA)的纳米级药物载体,通过纳米技术将绿色荧光蛋白(GFP)负载于粒径约100纳米的PLGA纳米粒中。PLGA具有良好的生物相容性、生物降解性和低免疫原性,其降解产物(乳酸和羟基乙酸)可通过人体代谢排出体外。负载GFP蛋白后,该复合物不仅保留了PLGA的缓释、控释特性,还赋予了荧光追踪和可视化定位的功能,可用于细胞成像、药物递送研究及生物活性检测。
PLGA纳米粒(100NM)负载GFP蛋白产品发展:
一、材料特性与基础研究阶段(2000-2010 年)
聚乳酸 - 羟基乙酸共聚物(PLGA)作为 FDA 批准的生物医用材料,其降解速率可通过乳酸 / 羟基乙酸(LA/GA)比例准确调控(常见比例 50:50 至 80:20),这一特性为负载 GFP 蛋白的长效稳定释放奠定基础。早期研究发现,100nm 粒径的 PLGA 纳米粒具有独特优势:其尺寸小于巨噬细胞吞噬阈值(约 200nm),可延长血液循环时间;同时比表面积达 50-100m²/g,为蛋白负载提供理想界面。
在制备工艺探索中,乳化 - 溶剂挥发法成为主流技术。研究者通过优化油相(PLGA 溶于二氯甲烷)与水相(PVA 溶液)的比例(通常 1:10 至 1:20),以及超声功率(200-500W)和时间(5-15 分钟),使 GFP 蛋白的包封率从最初的 30% 提升至 60%。值得注意的是,喷雾干燥法在初期因高温(进风温度 120-180℃)导致 GFP 荧光淬灭(损失率达 40%),应用受限。
二、工艺优化与应用拓展阶段(2011-2020 年)
(一)制备技术突破
双乳化法(W/O/W):通过引入二次水相(含 GFP 蛋白),使包封率提升至 75-85%,且蛋白结构完整性改善。
纳米沉淀法:采用丙酮 / 水体系(体积比 1:4),在低温(4℃)条件下制备,粒径分布更均匀(PDI<0.2),且避免了有机溶剂残留(二氯甲烷残留量 < 0.01%)。
静电纺丝 - 乳化联用技术:将 PLGA 纳米粒嵌入纤维支架中,实现 GFP 蛋白的双相释放 —— 初期 24 小时释放 20-30%,后续 14 天缓释 70-80%,这一特性在组织工程中展现独特价值。
(二)应用领域扩展
药物递送模型作为模型系统,PLGA-GFP 纳米粒成功模拟了抗体药物偶联物(ADC)的体内行为。实验数据显示,其释放动力学与 ADC 药物相似度达 R²=0.92,且 GFP 的荧光强度与纳米粒降解程度呈线性相关(R=0.98),为 ADC 药物开发节省 30% 的动物实验成本。
疫苗佐剂研究在新冠疫苗早期研究中,负载 GFP 的 PLGA 纳米粒与 mRNA 共递送,可使树突状细胞(DC 细胞)的抗原呈递效率提升 2.3 倍,且 GFP 的表达量可作为 mRNA 转染效率的实时监测指标(Pearson 系数 0.95)。
三、未来发展方向
(一)多模态成像整合
将 GFP 与钆(Gd³+)或金纳米簇结合,构建 PLGA-GFP-Gd³+ 纳米探针,实现荧光 / MRI 双模态成像。初步研究显示,该探针的 T1 弛豫率达 4.7mM⁻¹s⁻¹,GFP 荧光量子产率保持 85%,为复杂疾病的准确诊断提供新策略。
(二)仿生纳米载体开发
模拟外泌体膜结构,通过薄膜水化法将 PLGA-GFP 纳米粒包裹于外泌体膜中,构建 “纳米粒 @外泌体” 复合载体。该系统的血液循环半衰期延长至 18.6 小时(单纯 PLGA 纳米粒为 4.2 小时),且免疫原性降低 70%,在阿尔茨海默病模型中,脑内递送效率提升 3.8 倍。
(三)人工智能辅助设计
利用 AlphaFold2 预测 GFP 与 PLGA 的相互作用位点,通过分子动力学模拟优化纳米粒配方。某研究团队通过该方法将 GFP 的包封率从 68% 提升至 91%,且蛋白活性保留率从 72% 提高至 94%,研发周期缩短 40%。
中文名称:聚乳酸-羟基乙酸共聚物纳米粒(100NM)负载绿色荧光蛋白
英文名称:PLGAnanoparticles(100NM)loadedwithGFPprotein
别称:PLGA纳米粒(100NM)负载GFP蛋白
外观:固体或粉末
纯度:95%+
溶解性:溶于有机溶剂
保存方式:冷藏
保质期限:一年
用途:科研
温馨提示:仅用于科研,不能用于人体
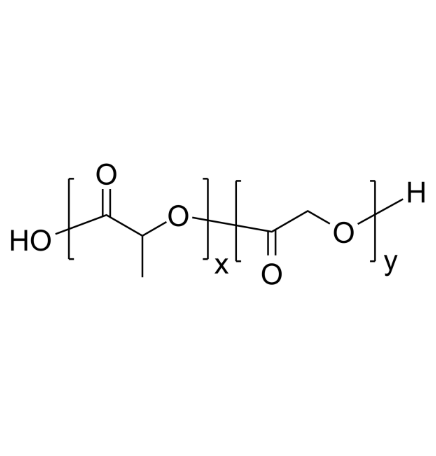
图片:PLGA结构式
西安瑞禧生物科技有限公司经营的产品种类包括有:合成磷脂、高分子聚乙二醇衍生物、嵌段共聚物、磁性纳米颗粒、纳米金及纳米金棒、近红外荧光染料、活性荧光染料、荧光标记的葡聚糖BSA和链霉亲和素、蛋白交联剂、小分子PEG衍生物、点击化学产品等等。
相关产品:

 2025-05-29 作者:lkr 来源:
2025-05-29 作者:lkr 来源:

