PLA-PEG-NH₂共聚物,融合了聚乳酸(PLA)的生物可降解性、聚乙二醇(PEG)的良好亲水性以及氨基(-NH₂)的化学活性,在生物医学领域展现出巨大的应用潜力,其可控合成及端氨基活性研究意义重大。
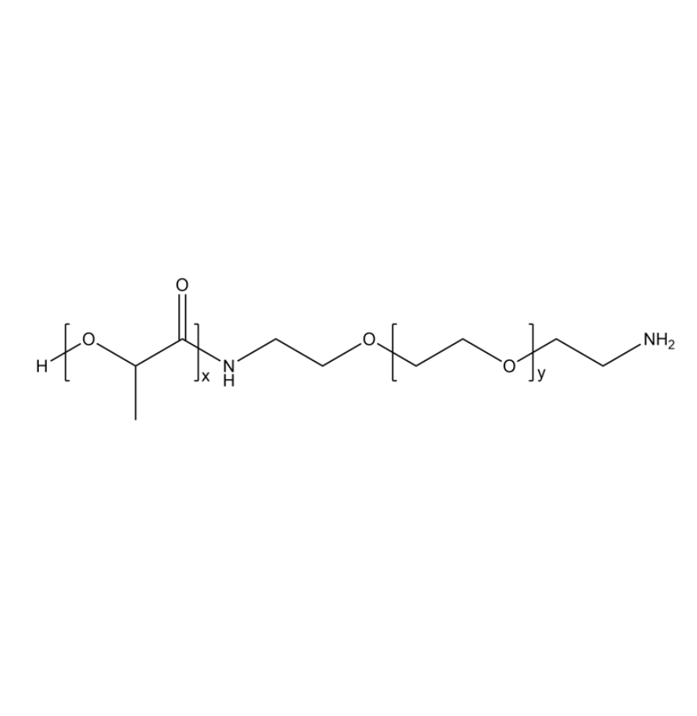
图为:PLA-PEG-NH2结构式
在合成方面,常见的方法有开环聚合法。以 PEG-NH₂为大分子引发剂,引发丙交酯(LA)单体进行开环聚合,逐步形成 PLA 链段。此过程中,通过准确控制反应条件,如温度、反应时间、引发剂与单体的比例等,可有效调控 PLA-PEG-NH₂共聚物的分子量及其分布。例如,适当升高温度并延长反应时间,能促使 LA 单体更多地参与聚合,增加 PLA 链段的长度,从而提升共聚物的分子量。同时,这种方法能较好地保留氨基的活性,为后续的功能化修饰奠定基础。另一种方式是先通过特定反应将末端炔基或叠氮基修饰的 PEG 与 PLA 链连接,之后再引入氨基,该途径适用于对功能基团位置有准确调控需求的情况。
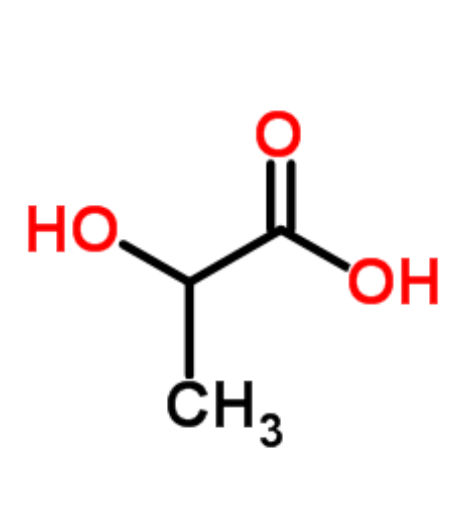
图为:聚乳酸结构式
端氨基的活性赋予了 PLA-PEG-NH₂共聚物性能。在靶向药物递送领域,利用氨基可与tumor特异性配体,如叶酸、Her2 抗体等进行偶联。这些配体如同 “导航仪”,能引导共聚物形成的纳米颗粒准确地富集于tumor部位,实现主动靶向,提高药物对tumor细胞的作用效果。此外,氨基还能通过阳离子修饰,例如季铵化引入正电荷,与带负电的核酸通过静电作用复合,形成稳定的纳米复合物,用于基因递送。同时,结合 pH 敏感键或酶切位点,借助氨基的反应活性构建相应结构,能够实现药物在tumor微酸性环境(pH 6.5-6.8)下的可控释放,减少对正常组织的副作用。
随着研究的不断深入,对 PLA-PEG-NH₂共聚物可控合成及端氨基活性的准确把握,将为其在生物医学领域,如高效药物递送系统构建、组织工程支架优化等方面,开辟更为广阔的应用前景。

 2025-07-04 作者:lkr 来源:
2025-07-04 作者:lkr 来源:

