生物正交化学自 2003 年由贝尔托西正式提出后,凭借其能在活体细胞内进行且与生物体内反应互不干扰的特性,在生物医学领域大放异彩。PEG-DBCO 作为生物正交化学中的明星试剂,发挥着关键作用。
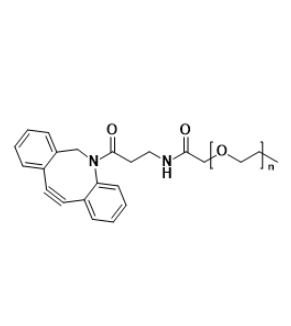
图为:PEG-DBCO结构式
PEG-DBCO 中的 DBCO 基团(二苯并环辛炔)是生物正交反应的核心参与者,它能与叠氮基团发生无铜催化的叠氮-炔环加成反应(SPAAC)。这种反应具有极高的选择性和反应活性,即使在复杂的生物体系中,也能快速且特异性地与含叠氮的生物分子结合。PEG(聚乙二醇)部分则赋予了分子良好的水溶性、生物相容性和低免疫原性,可减少试剂在生物体内的非特异性吸附,延长其在体内的循环时间,使生物正交反应更稳定、高效地进行。
在生物成像领域,PEG-DBCO 被应用于标记生物分子。先将叠氮基团修饰到目标生物分子,如蛋白质、核酸或糖类上,再引入 PEG-DBCO,二者发生 SPAAC 反应,使 PEG-DBCO 成功标记目标物。由于 PEG 的良好性质,标记后的生物分子能在生物体内稳定存在,而 DBCO 与叠氮反应后形成的稳定连接,确保标记不易脱落。通过检测 PEG-DBCO 携带的荧光基团,就能实现对目标生物分子在细胞或活体中的准确定位与动态追踪,为疾病的早期诊断和病理机制研究提供关键信息。
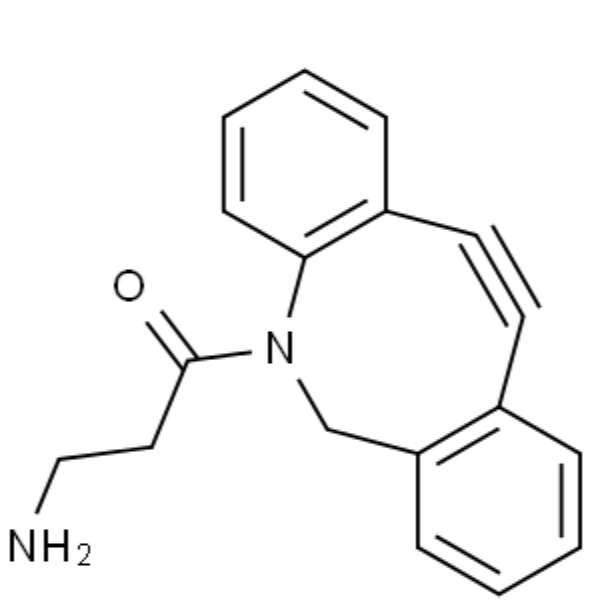
图为:DBCO结构式
药物递送方面,PEG-DBCO 也展现出独特优势。利用其与含叠氮修饰的药物载体或靶向分子特异性结合的特点,可构建高效、准确的药物递送系统。比如,将叠氮修饰在纳米颗粒表面,与 PEG-DBCO 反应后,能进一步连接具有靶向功能的配体,使纳米颗粒准确靶向病变组织。同时,PEG 的存在提高了药物载体的稳定性,减少药物在运输过程中的提前释放,提高药物Therapeutic effect 并降低副作用。
蛋白质修饰领域,PEG-DBCO 可用于定点修饰蛋白质。通过基因工程技术在蛋白质特定位置引入叠氮基团,再与 PEG-DBCO 反应,能将 PEG 链准确连接到蛋白质上,实现蛋白质的 PEG 化。这种准确修饰能改善蛋白质的稳定性、溶解性,延长其在体内的半衰期,还可避免传统随机 PEG 化对蛋白质活性的影响,为蛋白质类药物的研发和应用提供新策略。
随着研究深入,PEG-DBCO 在生物正交化学中的应用不断拓展创新。但目前仍面临一些挑战,如如何进一步优化其与生物分子的结合效率、降低成本等。相信随着技术的进步,PEG-DBCO 将在生物医学研究和临床应用中发挥更大作用,为攻克重大疾病带来新的希望。

 2025-07-21 作者:lkr 来源:
2025-07-21 作者:lkr 来源:

