文献:Ultrasound-Aided Targeting Nanoparticles Loaded with miR-181b for Anti-Inflammatory Treatment of TNF-α-Stimulated Endothelial Cells
文献链接:https://pubmed.ncbi.nlm.nih.gov/32715195/
作者:Donghong Liu, Jia Liu, Chao Li, Wei Li, Wei Wang, Jie Liu
相关产品:cRGDfC peptides cRGDfC肽
原文摘要:Gene therapy is an emerging therapeutic strategy used in clinics. Ultrasound-mediated gene transfection possesses great potential as a secure and available approach for gene delivery.
However, transfection efficiency and targeting ability remain challenging. In this study, we developed a kind of ultrasoundaided and targeting nanoparticles for microRNA delivery. These
nanoparticles carrying nucleic acids were prepared with cationic poly-(amino acid) encapsulated with perfluoropentane. The formulated nanoparticles were stabilized with negatively charged PGA−PEG−RGD peptide coating. Ultrasound imaging and specific gene transfection using this nanocarrier could be implemented simultaneously. Upon treatment with ultrasound irradiation, phase transition was induced in the nanoparticles and they generated acoustic cavitation, resulting in enhanced gene transfection against the endothelial cells. With the overexpression of miR-181b loaded by the nanoparticles, the TNF-α-stimulated endothelial cells were effectively rescued from the inflammatory state through the protection of cell viability and suppression of cell adhesion.
cRGDfC是一种具有特殊结构和功能的环肽,cRGDfC通过与细胞表面的αvβ3整合素结合,特异性地靶向tumor微Blood vessels和cancer细胞。作为一种有效且选择性的αvβ3整合素受体抑制剂,它在tumor具有重要应用。cRGDfC还可以用于生物成像领域,如磁共振成像(MRI)和光学成像等。通过与成像剂结合,可以实时监测tumor的生长和转移情况 。如果能够与 cRGDfC 竞争结合目标受体,并且抑制效果明显,说明该化合物可能具有较好的效果。同时,通过观察化合物对不同受体的选择性结合,可以评估其潜在的副作用和安全性风险。cRGDfC 在竞争抑制实验中具有应用,可以为受体 - 配体结合机制的研究以及化合物的有效性和安全性评估提供重要的实验依据。
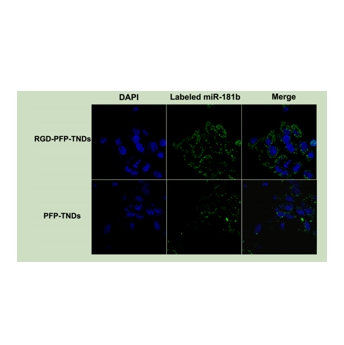
图为:与RGD−PFP-TNDs或PFP-TNDs孵育的HUVECs(DAPI染色)细胞核的CLSM图像
cRGDfC在竞争抑制实验中的应用:
用RGD多肽修饰的PFP-TNDs的主要功能是通过受体介导的细胞摄取来增强纳米颗粒向内皮细胞的选择性内化。为了研究RGD修饰的PFP-tnd的靶向作用,将HUVECs与不同浓度的游离cRGDfC肽预孵育,以阻断细胞膜上的RGD受体。随着游离cRGDfC多肽浓度的增加,RGD−PFP-TNDs组的细胞摄取效率和荧光素酶表达降低。相比之下,未经RGD修饰的tnd保持了相同的细胞摄取和基因转染效率。这种效应归因于阻断了现有受体介导的细胞对RGD−PFP-tnd的摄取。此外,PFP-TNDs组的平均荧光强度(MFI)高于RGD−PFP-TNDs;随着游离RGD浓度一定程度的增加,PFP-TNDs上修饰的额外RGD也影响了纳米颗粒与细胞之间的相互作用,与非RGD修饰的样品相比,这可能导致细胞摄取效率降低。
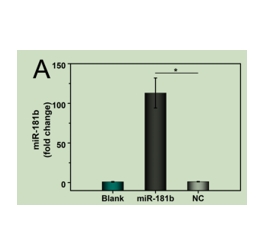
图为:用RGD−PFP-TNDs转染miR-181b或NC后的HUVECs中miR-181b的qPCR分析
结论:在竞争抑制实验中,cRGDfC 可以作为已知的配体与目标受体结合。通过加入不同浓度的 cRGDfC,可以观察其对另一种未知配体与受体结合的抑制作用。如果 cRGDfC 能够有效地竞争抑制未知配体与受体的结合,说明未知配体可能与受体具有相似的结合位点,从而为确定受体 - 配体结合的特异性提供重要线索。通过分析 cRGDfC 在竞争抑制实验中的浓度 - 效应关系,可以深入了解受体与配体的结合机制。例如,可以计算出 cRGDfC 的抑制常数(Ki),该常数反映了 cRGDfC 与受体的结合亲和力以及对未知配体结合的抑制能力。此外,还可以通过改变实验条件,如温度、pH 值等,观察 cRGDfC 在竞争抑制实验中的变化,进一步探讨受体结合的热力学和动力学特性。

 2025-07-28 作者:lkr 来源:
2025-07-28 作者:lkr 来源:

