在生物医学领域,羧基化聚乙二醇修饰的金纳米粒子凭借独特性质备受关注,探究其在生物体内的代谢与分布规律,对评估其生物安全性与拓展应用意义重大。
Au-PEG-COOH 中的金纳米粒子(Au NPs)作为核心,具有良好的稳定性、高电子密度及独特光学性质。聚乙二醇(PEG)链的修饰,极大提升了其水溶性与生物相容性,末端羧基(-COOH)则赋予其可修饰性,便于连接各类生物活性分子。
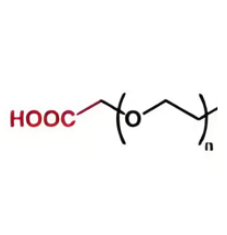
图为:Au-PEG-COOH结构式
当 Au-PEG-COOH 进入生物体后,首先面临的是体内复杂的生理环境。其在blood循环系统中的分布,受多种因素影响。PEG 链的空间位阻效应,可有效减少单核巨噬细胞系统(MPS)的识别与吞噬,延长其在blood中的循环时间。研究表明,相较于未修饰的金纳米粒子,Au-PEG-COOH 在blood中的半衰期明显延长,能在较长时间内维持一定浓度,这为其在体内的长程运输与作用发挥提供了基础。
在组织分布方面,Au-PEG-COOH 展现出独特特性。tumor组织由于存在高通透性和滞留效应(EPR),对 Au-PEG-COOH 具有一定的被动靶向性。纳米粒子可通过tumor组织的blood vessels间隙渗出并在tumor部位富集,为tumor成像与Treatment 提供了可能。同时,若在羧基位点连接tumor特异性靶向分子,如抗体、适配体等,可进一步增强其对tumor组织的主动靶向能力,实现准确定位。

图为:纳米颗粒
关于代谢过程,Au-PEG-COOH 相对稳定,金纳米粒子在生理条件下难以被降解。然而,PEG 链部分可在体内多种酶的作用下,发生缓慢的降解。PEG 降解产物为小分子聚乙二醇片段,最终可通过许多途径排出体外。相关研究通过追踪标记的 PEG 片段,证实了这一排泄途径。但整体而言,Au-PEG-COOH 在体内的代谢速率较为缓慢,这也确保了其在一定时间内维持结构完整性与功能稳定性。
尽管 Au-PEG-COOH 在生物体内代谢与分布表现出一定优势,但仍存在挑战。例如,长期低剂量暴露下的潜在累积效应尚不明确;不同粒径、表面电荷的 Au-PEG-COOH 在体内代谢与分布的差异,也有待深入研究。总体而言,明确 Au-PEG-COOH 在生物体内代谢与分布规律,有助于优化其设计,推动在生物医学领域的安全、有效应用,为疾病诊断与Treatment 带来更多突破。

 2025-06-16 作者:lkr 来源:
2025-06-16 作者:lkr 来源:

